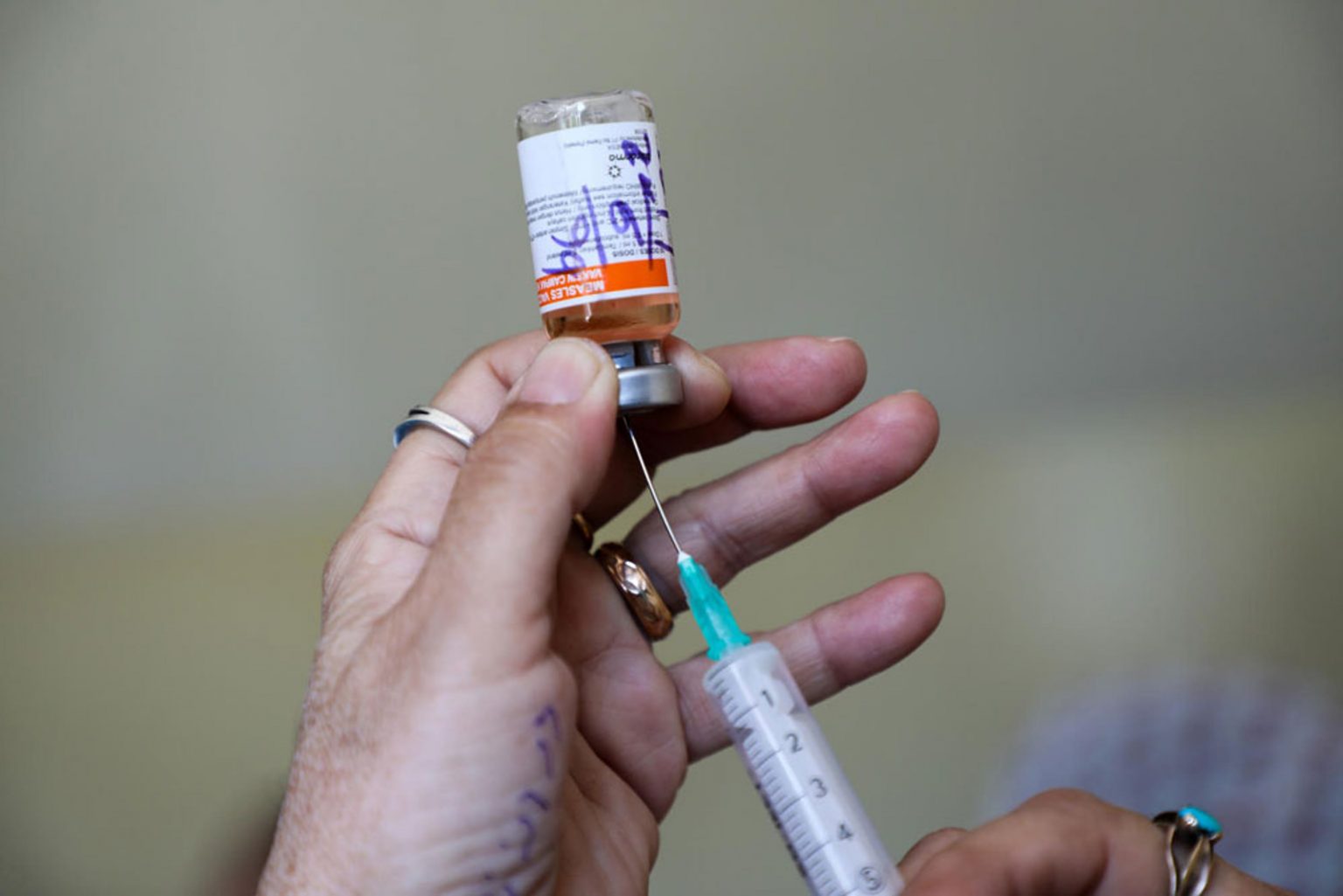
Trenta professori e ricercatori universitari americani chiedono l’accesso ai dati del vaccino Pfizer, in base al Freedom of Information Act: gli è stato risposto che lo avranno fra 55 anni. La parola “lockdown”, che speravamo di non sentire mai più, incombe intanto su tutta l’Europa, e davanti ai centri vaccinali vediamo nuove code per la...
Ripartono i lockdown e si anticipano le terze dosi. Cosa non torna nelle campagne vaccinali
Laura Calosso
Scrittrice, giornalista e traduttrice, laureata in Scienze Politiche e in Lettere, Culture moderne comparate, Letteratura tedesca. Ha lavorato come giornalista e addetta stampa. La carriera di scrittrice è iniziata con una menzione di merito al Premio Calvino, edizione 2008/2009, e il primo romanzo "A ogni costo, l'amore" pubblicato da Mondadori nel 2011. Il giornalismo d’inchiesta è la sua passione. Lavora nel mondo dell’editoria e per la Rai.